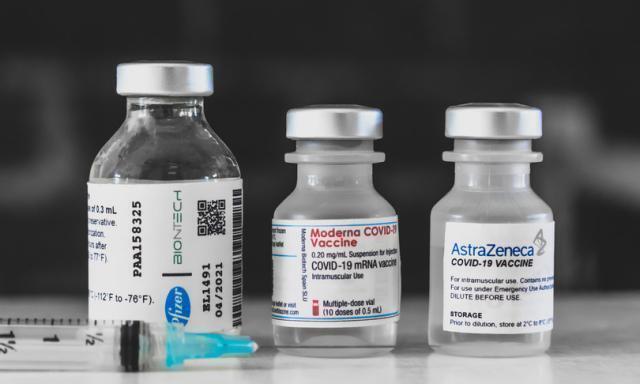
Da quello di Pfizer/BioNtech a quello di AstraZeneca, fino a Coronavac di Sinopharm, alcuni sieri sono già utilizzati o prossimi ad esserlo nelle campagne vaccinali. Per altri bisogna attendere la fine delle sperimentazioni e i via libera degli enti di controllo
– I vaccini di Pfizer, AstraZeneca e Moderna
Dopo il via libera al vaccino di Pfizer/Biontech in Europa, di quello AstraZeneca nel Regno Unito e in Argentina e del BBIBP-CorV, quello prodotto dal Beijing Biological Products Institute (Sinopharm) che ha ricevuto il via libera condizionato per il commercio dalla National Medical Products Administration (NMPA), l’agenzia del farmaco cinese, ora si attende per il prossimo 6 gennaio il verdetto del Comitato di valutazione dei farmaci ad uso umano (CHMP) dell’Agenzia Europea del farmaco (EMA) sul vaccino “mRNA-1273” di Moderna.
L’Ema, dopo le pressioni del Governo tedesco e le sollecitazioni della Commissione Europea, ha infatti deciso di anticipare proprio al 6 gennaio prossimo, la riunione che era inizialmente prevista per il 12 gennaio. Un eventuale via libera al vaccino di Moderna si aggiungerebbe a quelle già ottenute a dicembre dalla Food and Drugs Administration (FDA) e dall’agenzia di regolamentazione Health Canada. In attesa del verdetto dell’Ema, la Commissione Europea ha esercitato l’opzione per l’acquisto di ulteriori 80 milioni di dosi di “mRNA-1273” per gli Stati membri dell’Unione Europea, portando le dosi totali acquistate di mRNA-1273 di Moderna a 160 milioni.

Saranno sufficienti a vaccinare, al momento non più di 80 milioni di cittadini europei, dal momento che questo vaccino per essere efficace, richiede due dosi a distanza di qualche settimana.
In una situazione di stallo per quanto riguarda il mercato europeo è invece il vaccino di AstraZeneca, “Covid-19 AstraZeneca”, che ha appena ricevuto il via libera da parte della Medicines and Healthcare products Regulatory Agency (MHRA), l’autorità inglese di controllo del farmaco. In una nota diffusa ieri sera, l’Ema ha spiegato di aver acquisito fin qui già molti dati sul candidato vaccino prodotto anche in collaborazione con la Advent (Gruppo IRBM di Pomezia, Roma), sul quale è in atto la cosiddetta “rolling review”, una sorta di valutazione progressiva che avviene a mano a mano che arrivano i dati.
Finora, fanno sapere all’Ema, “sono state valutate alcune prove sulla sicurezza e l’efficacia provenienti da un’analisi aggregata dei dati clinici ad interim di quattro studi clinici in corso nel Regno Unito, Brasile e Sud Africa. L’ultimo pacchetto clinico è stato ricevuto il 21 dicembre ed è attualmente in fase di valutazione. Il CHMP ha già valutato i dati di studi di laboratorio (dati non clinici) e sta attualmente valutando i dati sulla qualità del vaccino (sui suoi ingredienti e sul modo in cui è prodotto)”.
I dati non sono però sufficienti, secondo gli esperti dell’agenzia del farmaco europea a “supportare il rigore richiesto per un’autorizzazione condizionata all’immissione in commercio e ciò è stato richiesto all’azienda”.
Si tratta dunque di una richiesta autorizzativa diversa da quella ottenuta dalla MHRA inglese che invece ha approvato un via libera al vaccino AstraZeneca in un contesto di uso di emergenza, in cui vengono valutati rischi e benefici derivanti dall’utilizzo del vaccino.
“Ulteriori informazioni – spiegano all’Ema dagli studi clinici in corso sono attese anche a partire da gennaio. I dati provvisori di un ampio studio in corso negli Stati Uniti sono previsti per il primo trimestre del 2021”.
Difficile, a questo punto immaginare che AstraZeneca possa ricevere tempestivamente il via libera in Ue e che l’azienda possa consegnare già entro i primi mesi del nuovo anno i vaccini opzionati dalla Commissione e dagli Stati membri, tra cui l’Italia, per il quale, il vaccino AstraZeneca, è determinante. Secondo il piano nazionale infatti, nel nostro paese sono attese più di 16 milioni di dosi del vaccino di Oxford, su un totale di oltre 28 milioni di dosi attese.
C’è anche un secondo vaccino che potrebbe non arrivare in tempo in Italia. Si tratta di quello prodotto dall’azienda tedesca Curevac, che secondo il piano messo a punto dal Commissario Arcuri, dovrebbe fornire poco più di due milioni di dosi entro il prossimo mese di marzo. Il vaccino è però ancora in sperimentale e soli il 21 dicembre scorso l’azienda ha fatto sapere di aver arruolato altri 3.600 volontari per lo studio di fase III grazie ad un coinvolgimento di tutto il personale della Clinica medica di Magonza in Germania.
Per far fronte a questo deficit nelle scorte vaccinali europee, lunedì la presidente della Commissione Europea, Ursula Von Der Leyen, ha annunciato l’acquisto di ulteriori 100 milioni di dosi del vaccino prodotto da Pfizer/Biontech che andranno ad integrare parzialmente le scorte destinate ai paesi membri.
Anche dalla Cina arrivano importanti novità sul fronte della corsa ai vaccini. Oggi la National Medical Products Administration (NMPA), l’agenzia del farmaco cinese ha rilasciato un’autorizzazione condizionata per il commercio al vaccino “BBIBP-CorV” prodotto dal Beijing Biological Products Institute, uno dei due vaccini che fanno capo al gruppo Sinopharm.
Il via libera arriva in vista delle vacanze del Capodanno Lunare previsto per l’11 febbraio, data entro la quale la Cina vuole iniziare a lanciare un’ampia campagna di immunizzazione della popolazione. Su questa strada però è arrivata come una doccia fredda la notizia che un altro produttore cinese di vaccini, Sinovac, ha ritardato la presentazione dei dati per il rilascio dell’autorizzazione condizionata al commercio per il suo “Coronavac”. Il ritardo è dovuto alla necessità di dover uniformare i dati sperimentali ottenuti nel corso di diversi trial che sono stati realizzati in Brasile, Indonesia, Cile e Turchia.
“I risultati della fase III rivelano che abbiamo raggiunto un numero di efficacia superiore a quanto necessario”, ha detto a BioWorld Dimas Covas, direttore dell’Istituto Butantan, l’istituo brasiliano che si occupa di gestire la sperimentazione del Brasile nel paese sudamericano. “Ora, l’idea è di rendere questi dati compatibili con i risultati dei test clinici dello stesso vaccino che vengono effettuati in altri paesi”.
Il ritardo nella presentazione dei dati potrebbe far slittare di qualche settimana l’autorizzazione da parte delle autorità cinesi e anche di quelle brasiliane che puntano molto su questo vaccino per contrastare la pandemia nel loro paese. Nonostante gli alti e i bassi dei diversi processi regolatori, sono ormai diversi i paesi che hanno iniziato le loro campagne di vaccinazioni. Israele è quello che ha avviato con maggiore determinazione la campagna che, al 30 dicembre ha già raggiunto il 9,8 per cento della popolazione con un totale di circa 794.000 dosi che hanno permesso di immunizzare una quota consistente – circa un terzo – della popolazione con età superiore a 60 anni.








